Для диагностики ТУБЕРКУЛЁЗА
Наборы реагентов «Амплитуб» для быстрой диагностики туберкулёза, в том числе с множественной и широкой лекарственной устойчивостью (МЛУ-ТБ, ШЛУ-ТБ).
В 2004 году по инициативе д.м.н., профессора Михаила Александровича Владимирского, заведующего сектором молекулярной диагностики туберкулёза НИИ Фтизиопульмонологии Первого МГМУ им. И.М.Сеченова, мы начали разработки в области ПЦР-диагностики туберкулёза.
«Амплитуб» — технология быстрой молекулярно-генетической диагностики туберкулёза для выявления микобактерий туберкулёзного комплекса, определения инфекционной опасности больного, определения антибиотикоустойчивости к препаратам I и II ряда, идентификации и генотипирования микобактерий.
Технология «Амплитуб» состоит из 3-х основных этапов: пробоподготовки, выделения ДНК и полимеразной цепной реакции (ПЦР) в реальном времени. Оригинальные технологические разработки нашей компании применяются на каждом из этих этапов и в совокупности обеспечивают высочайшую чувствительность, специфичность и информативность анализа, быстроту получения результатов и их высокую достоверность.
I этап
Пробоподготовка: в процессе инкубации с «Амплитуб-Преп» происходит инактивация микобактерий, разжижение и гомогенизация респираторных образцов.
II этап
Выделение ДНК: использование оригинальных реагентов и магнитных частиц обеспечивает получение максимального количества чистой ДНК и позволяет автоматизировать процесс выделения ДНК.
III этап
ПЦР в реальном времени: одновременная детекция нескольких различных участков генома комплекса микобактерий туберкулёза (МБТ) увеличивает информативность и достоверность анализа.
Преимущества технологии «АМПЛИТУБ»
Скорость
Технология «Амплитуб» позволяет сократить время, необходимое для обнаружения M.tuberculosis complex и определения лекарственной устойчивости с 1-3 месяцев до 1 дня в сравнении с традиционными культуральными методами.
Высокая достоверность результатов
Высокая достоверность результатов обеспечивается как на этапе обнаружения МБТ, так и на этапе определения антибиотикоустойчивости. Применение технологии «Амплитуб» позволяет обнаружить МБТ с высокой чувствительностью (не более 100 КОЕ/мл мокроты) и 100% специфичностью. Точное определение мутаций в наиболее значимых кодонах основных генов, ассоциирующихся с лекарственной устойчивостью к рифампицину и изониазиду, позволяет определить 90% антибиотикоустойчивых образцов со специфичностью, близкой к 100%
Безопасность
Клинические образцы инактивируются с помощью «Амплитуб-Преп» уже на этапе взятия и транспортировки биологического материала.
Возможность работы с клиническими образцами
Важным преимуществом технологии «Амплитуб» является возможность исследования не только культур микобактерий, но и непосредственно клинического материала (мокроты, промывных вод бронхов, спинномозговой жидкости, экссудата, пунктата, биоптата, мочи, отделяемого половых путей).
Автоматизация
Роботизированная станция TECAN и набор реагентов «М-Сорб-Туб-Автомат» позволяют полностью автоматизировать наиболее трудоёмкий этап выделения ДНК. Технология «Амплитуб» обеспечивает автоматический расчет результатов ПЦР-анализа с указанием количества выявленного возбудителя в образце и конкретных мутаций, определяющих устойчивость к антибиотикам.
I этап – Пробоподготовка, инактивация
«Амплитуб-Преп» (инактивирующий реагент) специально адаптирован для обработки мокроты. Обладает исключительными муколизирующими свойствами, благодаря которым может использоваться вместо раствора NALC-NaOH для обработки мокроты перед молекулярно-генетическими исследованиями.
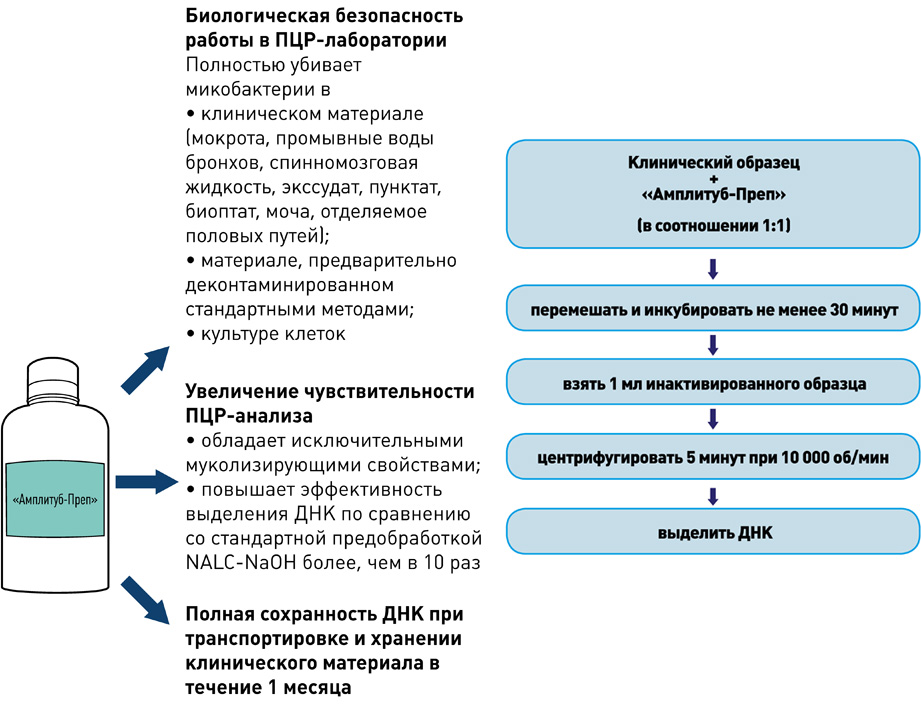
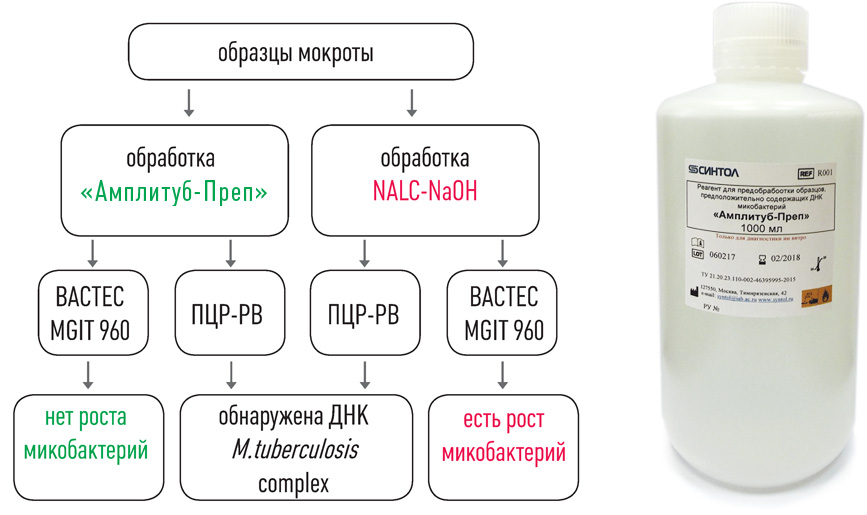
Клинические и технические испытания «Амплитуб-Преп» (инактивирующего реагента) проводились в ЦНИИ туберкулёза (Москва). 118 образцов мокроты от тяжёлых бациллярных больных с острым течением туберкулёза делили на две части, обрабатывали одну часть «Амплитуб-Преп», другую — NALC-NaOH.
Все образцы тестировали на BACTEC MGIT 960 и методом ПЦР в реальном времени (ПЦР-РВ). Рост микобактерий наблюдался только в контрольной группе, обработанной NALC-NaOH. В образцах, обработанных «Амплитуб-Преп», рост микобактерий не обнаружен. Результаты ПЦР-анализа образцов из обеих групп были положительными.
II этап – Выделение ДНК
Компанией «Синтол» разработан ряд наборов реагентов для выделения ДНК микобактерий.
«М-Сорб-Туб» («Амплитуб-РВ» комплект №1)
Набор реагентов для выделения ДНК (на магнитных частицах)
- Адаптирован для выделения ДНК микобактерий из мокроты, промывных вод бронхов, спинномозговой жидкости, экссудата, пунктата, биоптата, мочи, отделяемого половых путей, культур клеток.
- Набор «М-Сорб-Туб» обеспечивает лизис клеток, сорбцию ДНК на магнитных частицах, осаждение ДНК центрифугированием, промывку и элюцию ДНК.
- Предлагаемая компанией «Синтол» методика выделения ДНК сочетает в себе достоинства сорбционного метода и метода осаждения спиртом.
- Использование в качестве сорбента покрытых оксидом кремния магнитных частиц более удобно в сравнении с использованием других сорбентов, позволяет максимально стандартизировать и автоматизировать методику выделения ДНК.
- В каждый исследуемый образец добавляется внутренний положительный контроль (ВПК), по реакции амплификации ВПК судят о наличии/отсутствии ингибиторов ПЦР и эффективности выделения ДНК.
«М-Сорб-Туб-Автомат» («Амплитуб-РВ» комплект №1а; №1в)
Набор реагентов для выделения ДНК микобактерий из клинических образцов и культур клеток на автоматизированных станциях TECAN

Набор представляет собой модификацию набора реагентов «М-Сорб-Туб», разработанную специально для использования на автоматизированных станциях фирмы TECAN, что обеспечивает ряд следующих преимуществ.
- Снижение риска контаминации во время выделения ДНК практически до нуля.
- Значительное уменьшение трудоёмкости процесса выделения ДНК.
- Стандартизированное выделение ДНК из клинических образцов.
- Экономическая выгода: низкий расход пластика и реактивов.
«Экстра-Туб»
Набор реагентов для ускоренной пробоподготовки и выделения ДНК микобактерий из образцов мокроты
- Совмещение процесса пробоподготовки и выделения ДНК из образцов мокроты позволяет провести эти два этапа работы за 1 час.
- Минимальное количество манипуляций при пробоподготовке и выделении ДНК. Набор состоит из 3 рабочих растворов: «Амплитуб-Преп», лизирующего и элюирующего растворов.
- Использование «Амплитуб-Преп» в составе набора «Экстра-Туб» позволяет увеличить выход ДНК в 5‑10 раз.
III этап – ПЦР в реальном времени
Обнаружение и количественное определение комплекса МБТ
Набор реагентов АМПЛИТУБ-РВ — это:
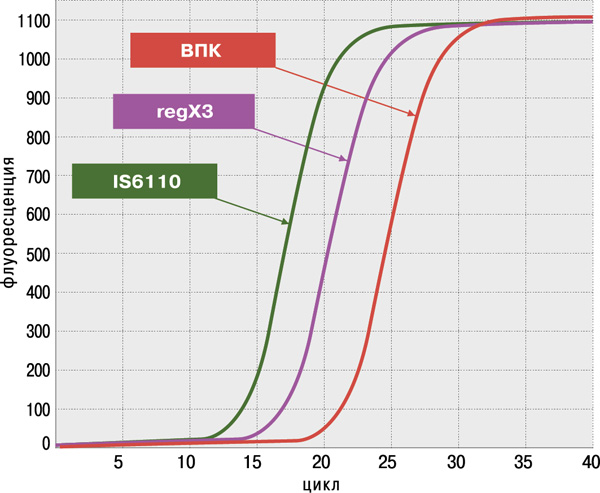
- высокая достоверность анализа благодаря одновременному обнаружению двух специфичных генов M.tuberculosis complex: IS6110 и regX3;
- оценка пригодности образца ДНК для определения антибиотикоустойчивости;
- высокая чувствительность (не более 100 КОЕ/мл мокроты или 1–10 копий фрагментов ДНК в реакции) и 100%‑ая специфичность, подтверждённые на панели QCMD (Quality Control for Molecular Diagnostics) Mtb EQA (UK).
Определение антибиотикоустойчивости МБТ к препаратам I и II ряда
Наборы реагентов АМПЛИТУБ-МЛУ-РВ, АМПЛИТУБ-FQ-РВ — это:
- диагностика форм туберкулеза с лекарственной устойчивостью, в том числе множественной лекарственной устойчивостью (МЛУ) и широкой лекарственной устойчивостью (ШЛУ);
- быстрая детекция мутаций M.tuberculosis, ассоциирующихся с устойчивостью к антибиотикам первого и второго ряда (рифампицину, изониазиду, этамбутолу, фторхинолонам);
- достоверность результатов, ежегодно подтверждаемая при проведении Федеральной службой внешней оценки качества (ФСВОК) Росздравнадзора испытаний шифрованных тест-культур и образцов.
Наборы АМПЛИТУБ-МЛУ-РВ и АМПЛИТУБ-FQ-РВ основаны на использовании оригинальной мультиконкурентной аллель-специфичной методики ПЦР в реальном времени, позволяющей выявлять мутации в генах микобактерий туберкулеза, ответственных за устойчивость к конкретным антибиотикам.
Ниже представлен перечень производимых нами наборов серии «Амплитуб»
- Амплитуб-Преп — реагент для предобработки образцов, предположительно содержащих ДНК микобактерий (кат.№R-001) Регистрационное удостоверение № РЗН 2017/6634
- АМПЛИТУБ-РВ — набор реагентов для для выделения, обнаружения и количественного определения ДНК микобактерий туберкулезного комплекса (кат. № ОМ-200а и ОМ-200ат (для автоматизированной станции TECAN)) Регистрационное удостоверение № ФСР 2010/07635.
- Амплитуб МБТК + НТМБ — набор реагентов для обнаружения ДНК микобактерий туберкулёзного комплекса (МБТК) и нетуберкулёзных микобактерий (НТМБ)
- АМПЛИТУБ-МЛУ-РВ — набор реагентов для определения лекарственной устойчивости микобактерий туберкулёзного комплекса к рифампицину и изониазиду методом ПЦР в реальном времени (кат. № ОМ-400) Регистрационное удостоверение № ФСР 2010/07636.
- АМПЛИТУБ-FQ-РВ — набор реагентов для выявления генетических маркеров ДНК микобактерий туберкулёзного комплекса, ассоциированных с устойчивостью к фторхинолонам, методом ПЦР в реальном времени (кат. № ОМ-800) Регистрационное удостоверение № РЗН 2017/5772
- АМПЛИТУБ-ДИФФЕРЕНЦИАЦИЯ — набор реагентов для дифференциации видов микобактерий, входящих в M.tuberculosis complex (M.tuberculosis, M.bovis, M.bovis BCG и др. виды) (кат. № ОМ-114)
- АМПЛИТУБ-Beijing — набор реагентов для определения генотипа Beijing микобактерий туберкулёза (кат.№ ОМ-115)
- «Экспресс-Туб» — набор реагентов для быстрого выделения ДНК микобактерий из культур клеток (кат. № ОМ-518)
В 2006 году в НИИ Фтизиопульмонологии Первого МГМУ им. И.М.Сеченова совместно с ЗАО «Синтол» был проведен скрининг более 2000 клинических образцов культур МБТ из 25 регионов Российской Федерации. Процент МЛУ-MБТ штаммов (к рифампицину и изониазиду), полученных от впервые выявленных пациентов, составил 21,9%, а процент MЛУ-MБТ штаммов, полученных от ранее леченных больных, был 58,5%. Совпадение результатов с данными микробиологическогоанализасоставило 94%. В рамках мониторинга был проведен молекулярно-генетический анализ диапазона и частоты встречаемости различных кодонов и мутаций в генах МБТ, ответственных за устойчивость к рифампицину и изониазиду.
В 2007 году проведены клинические испытания наборов по определению устойчивости к рифампицину и изониазиду.
В 2008–2011 годах проведена апробация наборов по определению устойчивости к препаратам резервного ряда (фторхинолонам, капреомицину, амикацину). В 2010 году разработан и испытан «Инактивирующий реагент А».
В настоящее время он продаётся под торговой маркой «Амплитуб-Преп».
В 2014–2017гг. в сотрудничестве с ФГБНУ «ЦНИИТ» разработан набор «Амплитуб-МБТК+НТМБ», позволяющий в 1 пробирке обнаружить ДНК микобактерий туберкулёзного комплекса и ДНК нетуберкулёзных микобактерий (без определения конкретного вида НТМБ).
В настоящее время ведётся разработка набора, позволяющего определять наиболее актуальные для российской популяции виды НТМБ.

Принцип мультиконкурентной аллель-специфичной методики ПЦР в реальном времени
- В формате одной пробирки используются 5’-флуоресцентно-меченые аллель-специфичные праймеры с общим комплементарным им 3’-меченым олигонуклеотидом-гасителем и контрольный флуоресцентный зонд, комплементарный участку ДНК без мутаций.
- При отсутствии мутаций в ДНК нарастание флуоресценции в ходе ПЦР-РВ наблюдается только по флуорофору зонда.
- При наличии мутаций в ДНК нарастание флуоресценции в ходе ПЦР-РВ наблюдается как по флуорофору зонда, так и по флуорофору 5’-флуоресцентно-меченого аллель-специфичного праймера. Данный метод позволяет определить не только точку мутации, но и процент устойчивого мутантного штамма МБТ на фоне дикого.
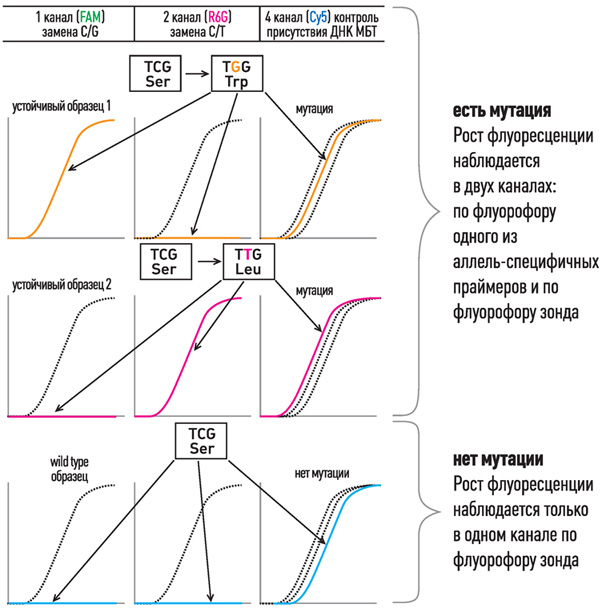
531 кодона rpoB гена M.tuberculosis
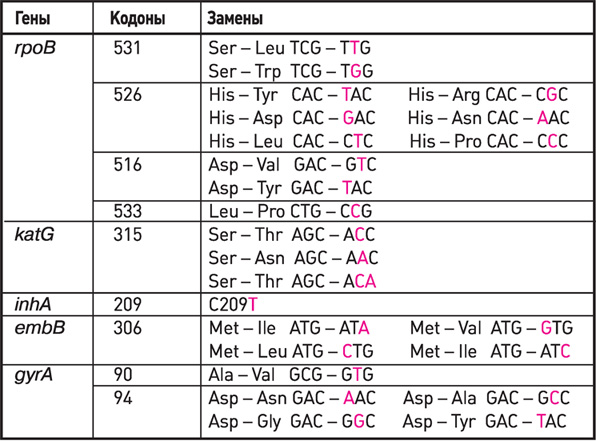
Гены, кодоны, замены, используемые в наборах реагентов
АМПЛИТУБ-МЛУ-РВ при определении антибиотикоустойчивости
Использование автоматизированных станций Freedom EVO (TECAN, Швейцария) для молекулярно-генетической диагностики туберкулёза
В 2011 году по инициативе сотрудников лаборатории молекулярно-генетических методов исследования ЦНИИТ РАМН группа разработчиков из ЦНИИТ под руководством профессора Черноусовой Ларисы Николаевны и «Синтола» впервые в России внедрила в лабораторную практику высокопроизводительную автоматизи-рованную систему выделения ДНК микобактерий на платформе Freedom EVO (TECAN) с использованием наборов реагентов «Амплитуб». Это позволило значительно сократить трудоёмкость ПЦР-диагностики туберкулёза и увеличить поток анализов.
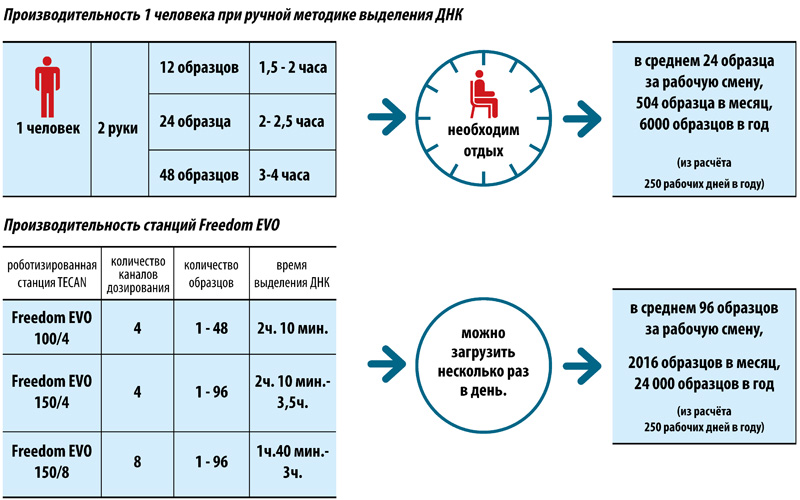
Время анализа МБТ при использовании автоматизированных станций Freedom EVO («TECAN», Швейцария) и наборов реагентов «Амплитуб» («СИНТОЛ», Россия)

Трудозатраты — 1 час
Продолжительность выделения ДНК — не более 2 часов
Подготовка к амплификации и ПЦР-РВ — 1,5 часа
ИТОГО: результаты анализа будут готовы через 3,5 часа
Оператор затратит 1 час своего рабочего времени.
Устройство автоматизированной станции Freedom EVO («TECAN», Швейцария) показано ниже:
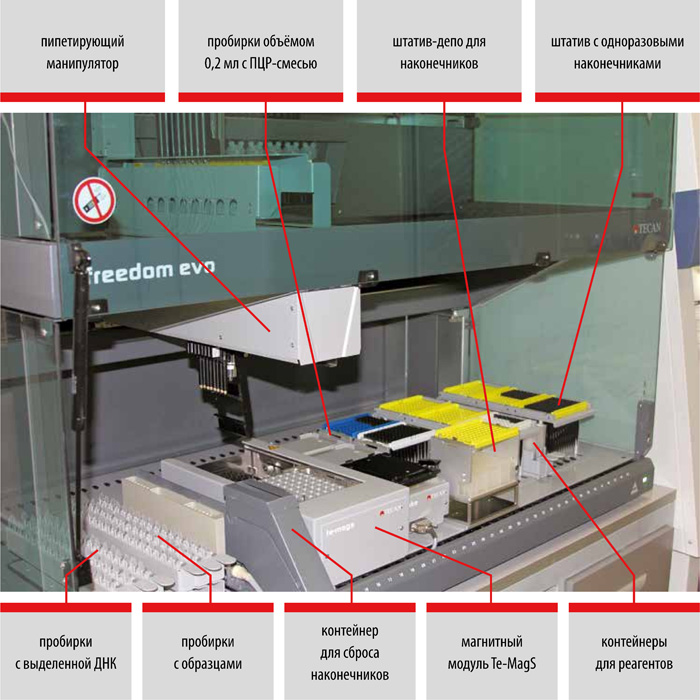
Выбирая технологию «Амплитуб» («Синтол») на платформе
Freedom EVO («TECAN»), Вы получаете:
- Обнаружение возбудителя туберкулёза — 48 образцов за 3 часа.
- Определение лекарственной устойчивости к препаратам I и II ряда за 1 день.
- Уменьшение трудозатрат в 6 раз.
- Увеличение производительности лаборатории.
- Безопасность работы благодаря «Амплитуб-Преп».
- Стандартизованное выделение ДНК.
- Снижение риска контаминации лаборатории.
- Низкую себестоимость 1 анализа.
- Признательность фтизиатров за быструю и точную диагностику!